O esquema representa o ciclo do nitrogênio:
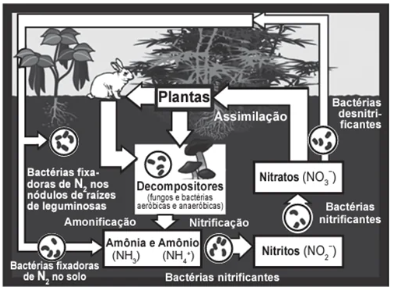
A chuva ácida interfere no ciclo do nitrogênio, principalmente, por proporcionar uma diminuição do pH do solo e da atmosfera, alterando a concentração dos compostos presentes nesse ciclo.
Disponível em: http://scienceprojectideasforkids.com. Acesso em: 6 ago. 2012 (adaptado).
Em um solo de menor pH, será favorecida a formação de:
A) N2
B) NH3
C) NH4+
D) NO2–
E) NO3
Solução
Dentre as substâncias apresentadas no esquema, a amônia (NH3), que é uma base fraca, o íon amônio (NH4+), que é um cátion formado a partir de uma base fraca, e íon NO2-, que é um ânion formado a partir de um ácido fraco, serão influenciados a partir variações de pH. Devemos considerar que quanto menor o pH do solo, maior a concentração de íons H+ presentes. Tais espécies estão envolvidas nos seguintes equilíbrios químicos:
1) NH3 + H+ ⇌ NH4+
2) HNO2 ⇌ H+ + NO2-
Seguindo o princípio de Le Chatelier, ao aumentarmos a concentração de uma espécie, o equilíbrio químico tende a se deslocar para o lado oposto em que aquela espécie se encontra, ou seja, no sentido de consumo. Portanto, se a concentração de H+ aumenta, o equilíbrio (1) desloca favorecendo a formação do íon NH4+, enquanto o equilíbrio (2) desloca para a direção que favorece a formação do HNO2. Portanto, concluímos que a formação do íon NH4+ será favorecida em solos mais ácidos.
Alternativa C






