Os esgotos domésticos são, em geral, fontes do íon tripolifosfato (P3O105−, de massa molar igual a 253 g mol−1), um possível constituinte dos detergentes. Esse íon reage com a água, como mostra a equação a seguir, e produz o íon fosfato (PO43−, de massa molar igual a 95 g mol−1), um contaminante que pode causar a morte de um corpo hídrico. Em um lago de 8 000 m3, todo o fósforo presente é proveniente da liberação de esgoto que contém 0,085 mg L−1 de íon tripolifosfato, numa taxa de 16 m3 por dia. De acordo com a legislação brasileira, a concentração máxima de fosfato permitido para água de consumo humano é de 0,030 mg L−1.
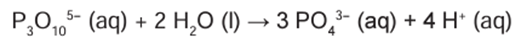
O número de dias necessário para que o lago alcance a concentração máxima de fósforo (na forma de íon fosfato) permitida para o consumo humano está mais próximo de
A) 158.
B) 177.
C) 444.
D) 1 258.
E) 1 596.
Solução
A taxa de liberação do íon tripolifosfato é de 16m3 por dia. Se o lago possui 8000 m3, o número de dias para o íon ocupar todo o volume do lago é dado por:
16m3 ———— 1 dia
8000 m3 ——– x
x = 500 dias.
Sabendo que todo fosfato (PO43-) é derivado do íon tripolifosfato (P3O105-), pela relação estequiométrica é possível descobrir o quanto de PO43- será formado a partir dos 0,085 mg L−1 de íon tripolifosfato
1 mol de P3O105- (massa 235 g/mol) forma 3 mol de PO43- (massa 95 g/mol)
P3O105- PO43-
235 g ————————– 285 g
0,085 mg L−1 —————- y
y = 0,096 mg L−1 de íons fosfato.
Os cálculos anteriores nos mostram que em 500 dias, a concentração do íon fosfato no lago dera de 0,096 mg L−1. Se o objetivo é saber o número de dias necessário para que o lago alcance a concentração máxima de fósforo (na forma de íon fosfato) permitida para o consumo humano, podemos pensar da seguinte forma:
0,096 mg L−1 de íons fosfato ———- 500 dias
0,030 mg L−1 de íons fosfato ———- z
z = 158 dias
Alternativa A






