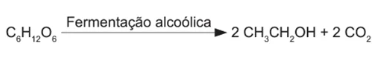
A obtenção de etanol utilizando a cana-de-açúcar envolve a fermentação dos monossacarídeos formadores da sacarose contida no melaço. Um desses formadores é a glicose (C6H12O6), cuja fermentação produz cerca de 50 g de etanol a partir de 100 g de glicose, conforme a equação química descrita.
Em uma condição específica de fermentação, obtém-se 80% de conversão em etanol que, após sua purificação, apresenta densidade igual a 0,80 g/mL. O melaço utilizado apresentou 50 kg de monossacarídeos na forma de glicose.
O volume de etanol, em litro, obtido nesse processo é mais próximo de
A) 16
B) 20
C) 25
D) 64
E) 100
Solução
De acordo com o enunciado, 100 g de glicose produzem 50 g de etanol. Entretanto, em uma condição específica de fermentação, o rendimento dessa reação é de 80%. Considerando a massa inicial de glicose de 50 kg (50.000 g), podemos calcular o quanto de etanol será obtido.
GLICOSE ETANOL
100 g ————– 50 g
50.000 g ———- x
x = 25.000 g de etanol (massa obtida sem levar em conta o rendimento)
ETANOL RENDIMENTO
25.000 g ——- 100%
y —————– 80%
y = 20.000 g de etanol (massa obtida a partir dos 50 kg iniciais de glicose)
A conversão da massa de etanol em volume pode ser feita a partir da densidade, em que
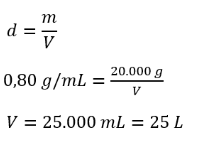
Alternativa C






