Grupos de pesquisa em todo o mundo vêm buscando soluções inovadoras, visando a produção de dispositivos para a geração de energia elétrica. Dentre eles, pode-se destacar as baterias de zinco-ar, que combinam o oxigênio atmosférico e o metal zinco em um eletrólito aquoso de caráter alcalino. O esquema de funcionamento da bateria zinco-ar está apresentado na figura.
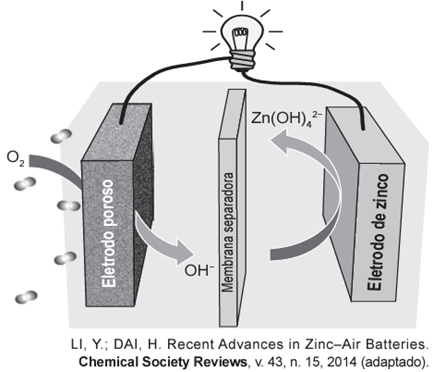
No funcionamento da bateria, a espécie química formada no ânodo é
A) H2 (g).
B) O2 (g).
C) H2O (l).
D) OH− (aq).
E) Zn(OH)42− (aq).
Solução
No contexto eletroquímico, o ânodo é o eletrodo no qual ocorre a oxidação (perda de elétrons), enquanto no cátodo ocorre a redução (ganho de elétrons).
Pelo esquema fornecido, observamos que no eletrodo poroso entra O2 (com número de oxidação do oxigênio igual a 0) e sai OH– (com o número de oxidação do oxigênio igual a -2). Isso indica que o oxigênio sofreu redução. Portanto, o eletrodo poroso é classificado como cátodo.
Por outro lado, o zinco metálico possui número de oxidação igual a 0. E na espécie formada, Zn(OH)42-, o zinco apresenta número de oxidação igual a +2, indicando que perdeu elétrons (foi oxidado). Assim, o eletrodo de zinco é o ânodo e o produto da reação é o íon Zn(OH)42-.
Alternativa E






