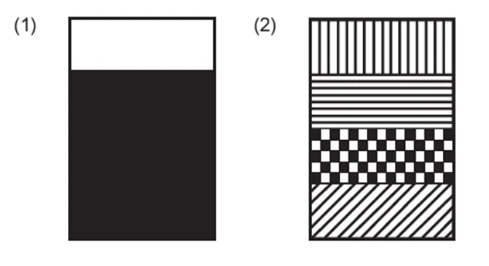
As figuras mostram dois experimentos. No primeiro, foram colocados em um frasco e agitados com uma colhervolumes iguais de mel, água, óleo e álcool etílico. Após alguns minutos, podia-se verificar que o sistema tinha duas fases (1). No segundo experimento, foram colocados, lentamente e sem agitação, os mesmos volumes de mel, água, óleo e álcool etílico. Pôde-se observar que, dependendo da ordem de adição de cada componente, o sistema permaneceu com quatro fases (2).
As propriedades de líquidos e soluções que justificam os resultados obtidos nos experimentos 1 e 2 são
A) solubilidade e densidade.
B) densidade e viscosidade.
C) viscosidade e solubilidade.
D) miscibilidade e viscosidade.
E) solubilidade e miscibilidade.
Solução
Em uma mistura, o que dita o número de fases presentes é a solubilidade de um componente em outro. Por outro lado, a densidade indica quais componentes da mistura têm tendência a se posicionar na parte inferior do recipiente e quais na parte superior.
Considerando o experimento 1, realizado sob intensa agitação, água, álcool etílico e mel são miscíveis entre si e formam uma fase única com maior densidade. O óleo, por não interagir com a fase aquosa e ser menos denso, se posiciona na parte superior do recipiente.
No experimento 2, no qual os componentes foram adicionados lentamente e sem agitação, a ordem de densidade dos componentes é a seguinte: mel > água > óleo > álcool etílico. Assim, o componente de maior densidade, o mel, ocupa o fundo do recipiente, seguido pela água, óleo e álcool etílico em ordem crescente de densidade.
Alternativa A






