Um bafômetro simples consiste em um tubo contendo uma mistura sólida de dicromato de potássio em sílica umedecida com ácido sulfúrico. Nesse teste, a detecção da embriaguez por consumo de álcool se dá visualmente, pois a reação que ocorre é a oxidação do álcool a aldeído e a redução do dicromato (alaranjado) a cromo(III) (verde) ou cromo(II) (azul).
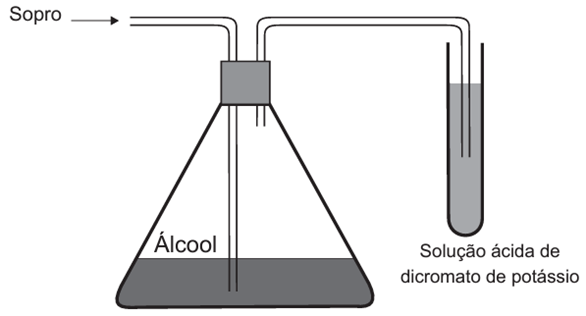
A equação balanceada da reação química que representa esse teste é:
A) Cr2O72− (aq) + 2 H+ (aq) + 3 CH3–CH2–OH (g) → 2 Cr2+ (aq) + 4 H2O (l) + 3 CH3–COOH (g)
B) Cr2O72− (aq) + 8 H+ (aq) + 3 CH3–CH2–OH (g) → 2 Cr3+ (aq) + 7 H2O (l) + 3 CH3–CHO (g)
C) CrO42− (aq) + 2 H+ (aq) + 3 CH3–CH2–OH (g) → Cr3+ (aq) + 4 H2O (l) + 3 CH3–CHO (g)
D) Cr2O72− (aq) + 8 H+ (aq) + 3 CH3–CHO (g) → 2 Cr3+ (aq) + 4 H2O (l) + 3 CH3–COOH (g)
E) CrO42− (aq) + 2 H+ (aq) + 3 CH3–CHO (g) → Cr2+ (aq) + H2O (l) + 3 CH3–COOH (g)
Solução
Conforme descrito pelo enunciado, a reação que ocorre envolve a oxidação do álcool para aldeído e a redução do íon dicromato (de cor alaranjada) para cromo(III) ou cromo(II).
Nas alternativas A, D e E um dos produtos formados é um ácido carboxílico (ácido etanoico), o que não é compatível com a descrição fornecida e, portanto, podem ser desconsideradas.
O íon dicromato possui a fórmula Cr₂O₇²⁻, o que faz da alternativa B a única opção correta, uma vez que o íon mencionado na alternativa C é o cromato (CrO₄²⁻).
Alternativa B






