O alumínio é um metal bastante versátil, pois, a partir dele, podem-se confeccionar materiais amplamente utilizados pela sociedade. A obtenção do alumínio ocorre a partir da bauxita, que é purificada e dissolvida em criolita fundida (Na3AlF6) e eletrolisada a cerca de 1 000 °C. Há liberação do gás dióxido de carbono (CO2), formado a partir da reação de um dos produtos da eletrólise com o material presente nos eletrodos. O ânodo é formado por barras de grafita submergidas na mistura fundida. O cátodo é uma caixa de ferro coberta de grafita. A reação global do processo é:
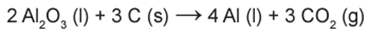
Na etapa de obtenção do alumínio líquido, as reações que ocorrem no cátodo e ânodo são:
Solução
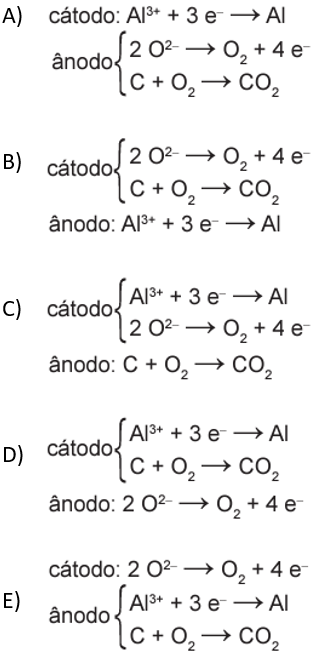
A partir da análise da equação de oxirredução, pode-se perceber que o alumínio sofre redução r as reduções são sempre catódicas. No ânodo, os íons O²⁻ serão oxidados para formar oxigênio molecular (O₂), que posteriormente oxida o eletrodo de carbono formando CO2.
Cátodo (redução): Al3+ +3 e−→ Al
Ânodo (oxidação): 2 O2−→ O2 + 4e−
Reação do eletrodo de carbono: C + O2 → CO2
Alternativa A






