Após seu desgaste completo, os pneus podem ser queimados para a geração de energia. Dentre os gases gerados na combustão completa da borracha vulcanizada, alguns são poluentes e provocam a chuva ácida. Para evitar que escapem para a atmosfera, esses gases podem ser borbulhados em uma solução aquosa contendo uma substância adequada. Considere as informações das substâncias listadas no quadro.
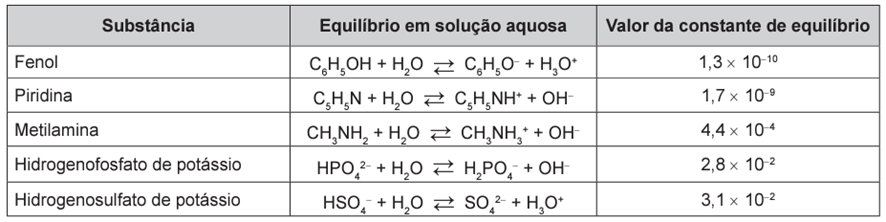
Dentre as substâncias listadas no quadro, aquela capaz de remover com maior eficiência os gases poluentes é o(a)
A) fenol.
B) piridina.
C) metilamina.
D) hidrogenofosfato de potássio.
E) hidrogenosulfato de potássio.
Solução
A combustão completa da borracha vulcanizada resulta na produção de dióxido de enxofre (SO2) e trióxido de enxofre (SO3), que são dois dos principais óxidos causadores da chuva ácida. Estes óxidos de caráter ácido, ao reagirem com a água, formam ácido sulfuroso e ácido sulfúrico, respectivamente, o que contribui para o aumento da acidez da chuva. Para neutralizar a acidez e remover esses gases poluentes, é necessário um composto que libere íons OH−, que podem neutralizar os íons H3O+ (H+) gerados pelos ácidos.
Dentre os compostos que liberam íons OH−, o hidrogenofosfato de potássio é o mais eficaz, pois possui a maior constante de equilíbrio, tornando-o o agente mais adequado para a remoção desses gases poluentes.
Ter a maior constante de equilíbrio significa que, para uma reação química específica, o equilíbrio se desloca (favorece) mais os produtos do que os reagentes. Portanto, em relação ao problema proposto, quanto maior a constante de equilíbrio, maior a concentração de OH– no meio.
Alternativa D






