O bisfenol-A é um composto que serve de matéria-prima para a fabricação de polímeros utilizados em embalagens plásticas de alimentos, em mamadeiras e no revestimento interno de latas. Esse composto está sendo banido em diversos países, incluindo o Brasil, principalmente por ser um mimetizador de estrógenos (hormônios) que, atuando como tal no organismo, pode causar infertilidade na vida adulta. O bisfenol-A (massa molar igual a 228 g/mol) é preparado pela condensação da propanona (massa molar igual a 58 g/mol) com fenol (massa molar igual a 94 g/mol), em meio ácido, conforme apresentado na equação química.
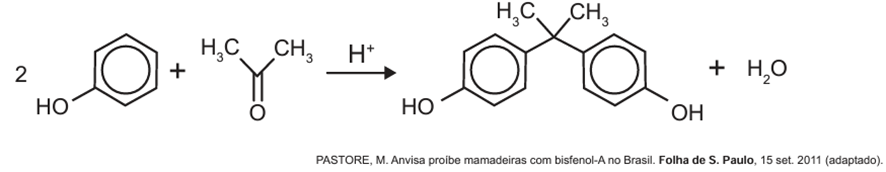
Considerando que, ao reagir 580 g de propanona com 3 760 g de fenol, obteve-se 1,14 kg de bisfenol-A, de acordo com a reação descrita, o rendimento real do processo foi de
A) 0,025%.
B) 0,05%.
C) 12,5%.
D) 25%.
E) 50%.
Solução
Como foi dada a massa dos dois reagentes, precisamos calcular o excesso e limitante. Pela estequiometria, 2 mol de fenol reagem com 1 mol de propanona. Sendo assim, temos:
2 mol de fenol 1 mol de propanona
2 94 g ———————– 58g
x ——————————– 580 g
x = 1 880 g de fenol.
A massa de 1.880 g encontrada é a quantidade necessária de fenol para reagir com 580 g de propanona. No entanto, foram utilizados 3.760 g de fenol, indicando que há um excesso desse reagente. O excesso de fenol não pode ser considerado para cálculos posteriores. Portanto, a relação a ser utilizada para o próximo cálculo deve ser estabelecida entre a propanona e o bisfenol-A.
OBS: para calcular o excesso/limitante utilizando esse raciocínio, o “x” pode ser tanto para obter a massa de propanona, quanto do fenol. O que vale é a interpretação do resultado.
Novamente, pela estequiometria, 1 mol de propanona forma 1 mol de bisfenol-A. O cálculo seguinte fornecerá a quantidade esperada de bisfenol-A formada a partir de 580 g de propanona. Sendo assim, temos que:
1 mol de propanona 1 mol de bisfenol-A
58 g ——————————- 228 g
580 ——————————– y
y = 2 280 g de bisfenol-A (2,28 kg).
A massa final esperada de bisfenol-A é de 2,28 kg. Se foram obtidos somente 1,14 kg, o rendimento é de:
2,28 kg ————– 100%
1,14 kg ————– R
R = 50%
Alternativa E






